张京莉,郑志慧,杨连任,李志强,孙步伟
非小细胞肺癌(NSCLC)的治疗已进入到针对驱动基因的分子靶向精准治疗时代。NSCLC 最常见的驱动基因是表皮生长因子受体 (epidermal growth factorreceptor,EGFR)突变,激活EGFR 信号通路,导致肿瘤形成[1]。
EGFR 基因的突变在亚洲NSCLC 患者中比例远高于高加索裔NSCLC 患者,尤其在亚洲无吸烟史的肺腺癌女性患者中比例高达60%[2-3]。第一代和第二代EGFR 酪氨酸激酶抑制剂(TKI)做为EGFR 敏感突变的NSCLC 患者的一线治疗方案,无疾病进展生存期(PFS)等较标准含铂双药化疗方案明显延长,然而几乎所有患者不可避免地会发生耐药肿瘤进展, 主要的耐药机制为T790M 突变[4]。第三代EGFR-TKIs 奥希替尼对T790M 突变和EGFR 致敏突变均有强效抑制作用, 国外多个指南已将其作为EGFR 突变阳性NSCLC 患者的首选一线治疗药物[5-6]。
奥希替尼2017 年在中国上市,但目前关于奥希替尼一线与序贯治疗中国NSCLC 患者比较的真实世界研究相对缺乏。
因此,本研究回顾性收集EGFR 突变晚期NSCLC 患者的治疗数据,比较奥希替尼一线与序贯治疗晚期NSCLC 患者的疗效、安全性。
1.1对象 选取2017 年5 月~2020 年2 月在皖南医学院附属太和医院行一代TKI 吉非替尼治疗进展后序贯奥希替尼治疗(序贯组47 例)和奥希替尼一线治疗(一线组24 例)的EGFR 突变阳性晚期NSCLC 患者临床数据。
纳入标准:(1)IIIB 或IV 期NSCLC;
(2) 经二代测序或ARMS 证实存在EGFR阳性突变;
(3)影像学等评估资料完整。
排除标准:(1) 在获知基因检测结果前接受过其他方案治疗;
(2)联合放化疗等其他治疗手段;
(3)合并其他恶性肿瘤。
1.2方法 序贯组口服吉非替尼(阿斯利康,国药准字J20180014)250 mg/次、1 次/d,耐药后确认存在T790M 序贯口服奥希替尼 (阿斯利康, 国药准字J20180027)80 mg/次、 1 次/d。
一线组口服奥希替尼80 mg/次、 1 次/d。
1.3疗效评价 随访截止日期为2022 年2 月25日。
疗效评价按照实体瘤疗效评价标准(RECIST)1.1。
主要研究终点为疾病控制率(DCR)、客观缓解率(ORR)和无进展生存期(PFS)。
完全缓解(CR)为病灶完全消失;
部分缓解(PR)为病灶的最长径总和减小≥30%;
稳定(SD)为病灶的最长径总和减小<30%或增长<20%;
进展(PD)为病灶最长径的总和增加≥20%。DCR 为CR、PR、SD 患者之和占全部患者百分比。
ORR 为CR 与PR 患者之和占全部患者百分比。
PFS 序贯组为开始吉非替尼治疗时间至序贯使用奥希替尼出现PD 的时间或随访中止时间;
一线组为奥希替尼开始治疗至PD 的时间或随访中止时间。
记录患者不良反应,计算随访截止日两组的死亡率。
1.4统计学处理 采用SPSS 25.0 软件进行数据分析。
两组间DCR 等率的比较采用卡方检验,计量资料以(±s)表示,组间比较采用独立样本t检验,不良反应发生率采用秩和检验,PFS 采用Kaplan-Meier 法进行分析,并绘制生存曲线。
以P<0.05 为差异存在统计学意义。
2.1患者一般资料 两组性别、年龄、ECOG 评分、病理类型、临床分期、EGFR 突变类型比较,差异无统计学意义(P>0.05)。
一线组脑转移比例高于序贯组,差异有统计学意义(P<0.05)。
见表1。
表1 两组非小细胞肺癌患者基线资料(例,± s)
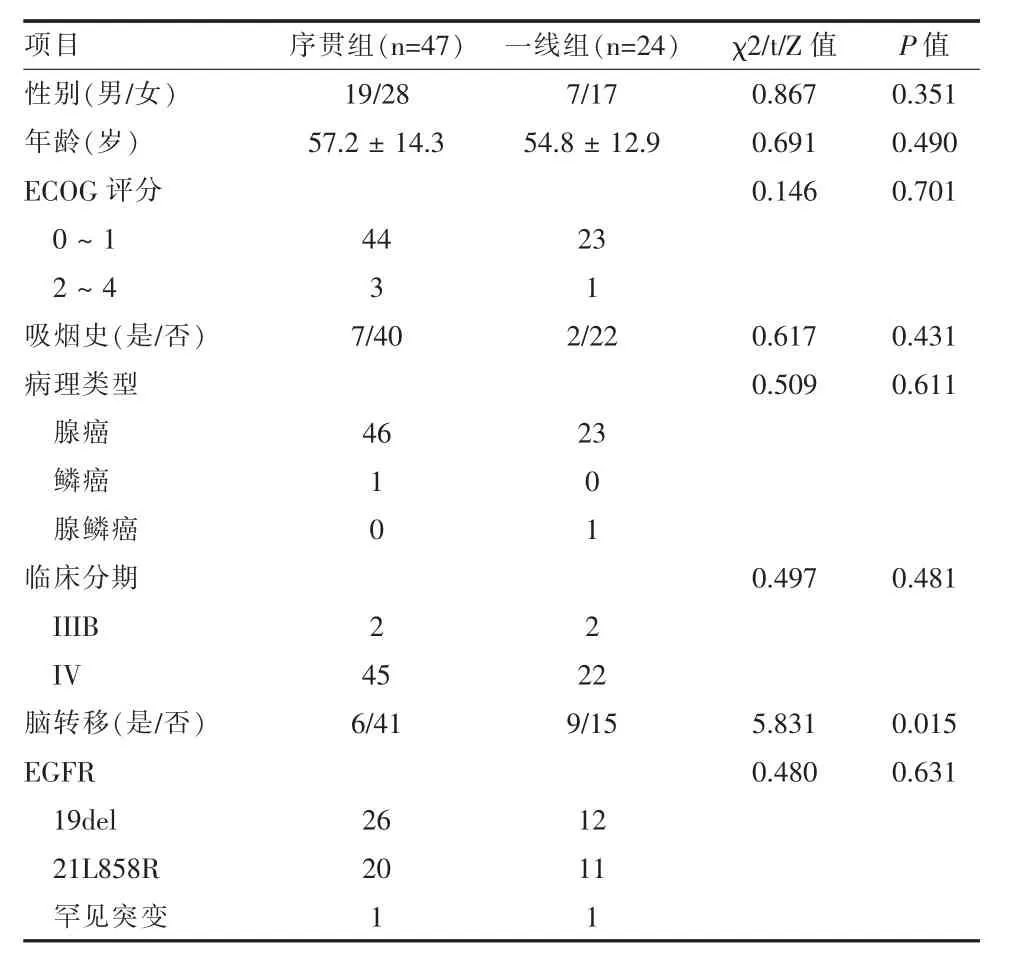
表1 两组非小细胞肺癌患者基线资料(例,± s)
?
2.2近期疗效比较 两组ORR 为70.21%vs.75.0%,DCR 为89.36%vs.91.66%, 序贯组略低于一线组,但组间差异无统计学意义(P>0.05)。
2.3远期疗效比较 序贯组中位PFS 为18.6 个月,一线组中位PFS 为17.8 个月,两年生存率序贯组为10.63%(5/47),一线组生存率41.66%(10/24),两组差异有统计学意义(χ2=9.179,P=0.002)。
2.4安全性分析 一线奥希替尼组3 级以上不良反应发生率12.5%(3/24),低于序贯组的23.4%(11/47),但组间差异无统计学意义(P>0.05)。
两组3级以下不良反应发生率及总不良反应发生率差异无统计学意义(P>0.05,表2)。

表2 两组非小细胞肺癌患者不良反应(例次)
第一、 二代EGFR-TKIs 主要的耐药机制为T790M 突变,降低了TKI 与三磷酸腺苷(ATP)可逆性竞争的能力。奥希替尼对T790M 突变细胞系的磷酸化仍有强效的抑制作用,其对经一、二代EGFRTKI 治疗后T790M 阳性的EGFR 敏感突变晚期NSCLC 患者疗效确切。FLAURA 研究比较了一线应用奥希替尼与第一代EGFR-TKI 厄洛替尼或吉非替尼治疗EGFR 突变阳性的晚期NSCLC 患者的疗效[7]。
FLAURA 研究中近半数的一代EGFR-TKI 治疗组患者在T790M 突变疾病进展后被交叉入组到奥希替尼组,在如此之高的交叉比例情况下,一线应用奥希替尼的患者OS 依然具有显著的优势[8]。
本研究因观察时限影响,总生存(OS)未统计,在随访截止日期时虽PFS 差异不显著,但一线组两年生存率高于序贯组。
这可能与以下因素有关:序贯组患者耐药后需确认T790M 突变,患者需要重新进行组织活检或血浆循环肿瘤DNA 检测。
有创性活检患者接受度差,ctDNA 检测假阴性率高, 可能延误T790M 突变患者的治疗时机。
此外,研究发现一线奥希替尼治疗后疾病进展类型中无快速进展病例,这说明奥希替尼未引发肿瘤生物学行为的恶化[9]。
一线奥希替尼耐药后不会出现T790M 突变,耐药机制包括C797S 单突变、MET 扩增突变等;
而二线服用奥希替尼耐药的机制比较复杂, 会出现C797S 与T790M 共突变等[10]。因此一线使用奥希替尼治疗可以减少复杂耐药的出现,在一线即选择奥希替尼治疗更有利于改善患者预后。
EGFR 突变主要包括EGFR 19 外显子缺失突变 (19Del) 和21 外显子L858R 突变(21L858R),FLAURA 研究是对21L858R 和19Del 进行了分层,避免了两种突变类型对患者EGFR-TKI 反应的差异导致偏倚。
本研究中一线组病例数偏少,再进行21L858R 和19el 分层各亚组病例数过低可能影响统计结果的准确性, 且基线资料比较, 两组的21L858R、19Del 比例差异无统计学意义。
故未进行分层比较。
FLAURA 研究中19Del 的患者治疗效果更好。母予馨[11]也报道T790M 突变合并19Del 的患者疗效优于合并21L858R 突变患者。
Jackman 等[12]对使用吉非替尼或厄洛替尼治疗的19Del 和L858R NSCLC 患者进行分层比较,发现与L858R 突变患者相比,19Del 患者的生存期更长。一代与三代EGFRTKI 治疗L858R 和19Del 突变的结果相似。
但为什么19Del 对EGFR-TKI 的抑制作用更加敏感, 仍需进一步机制研究。
总之,与一代酪氨酸激酶抑制剂序贯奥希替尼相比,奥希替尼一线治疗可提高生存率,降低不良反应使患者获益。
猜你喜欢耐药进展差异HIV相关淋巴瘤诊治进展传染病信息(2022年3期)2022-07-15JT/T 782的2020版与2010版的差异分析汽车实用技术(2022年10期)2022-06-09相似与差异音乐探索(2022年2期)2022-05-30非新生儿破伤风的治疗进展中国典型病例大全(2022年12期)2022-05-13如何提高医务人员对多重耐药菌感染防控措施执行率中国典型病例大全(2022年7期)2022-04-22滇藏铁路丽香段站后工程建设取得重要进展 有望年内开通云南画报(2022年3期)2022-04-19儿童医院临床分离多重耐药菌的流行病学分析昆明医科大学学报(2022年1期)2022-02-28miR-181a在卵巢癌细胞中对顺铂的耐药作用昆明医科大学学报(2022年1期)2022-02-28Micro-SPECT/CT应用进展现代仪器与医疗(2021年4期)2021-11-05找句子差异小天使·一年级语数英综合(2019年8期)2019-08-27